üĒį┤Ż║ŠWĮj┘Yį┤ 2022-11-14 21:04:42
ę╗Īó╦ß╝░╦ߥ─╗»īWąį┘|
╦ßį┌╦«╚▄ę║ųą─▄ĮŌļx│÷Üõļxūė(H+)║═╦ßĖ∙ļxūėĪŻ│ŻęŖĄ─╦ßėąó┘¹}╦ß(HCl)ó┌┴“╦ß(H2SO4) ó█Ž§╦ß(HNO3)ó▄┤ū╦ß(CH3COOH)
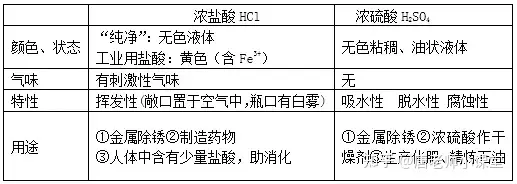
ó┘ūŽ╔½╩»╚’įćę║ė÷╦ßūā╝tŻ¼¤o╔½Ęė╠¬įćę║ė÷╦ß▓╗ūā╔½ĪŻ
ó┌╗ŅØŖĮī┘+╦ß¹}+ÜõÜŌ(ūóŻ║┤╦╠Ä╦ß▓╗░³└©ØŌ┴“╦ß║═Ž§╦ß)
Zn+H2SO4=ZnSO4+H2 Zn+2HCl=ZnCl2+H2
Fe+H2SO4=FeSO4+H2 Fe+2HCl=FeCl2+H2
2Al+3H2SO4=Al2(SO4)3+3H2
2Al+6HCl=2AlCl3+3H2
ó█Įī┘č§╗»╬’+╦ß¹}+╦«
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+H2SO4=CuSO4+H2O
CuO+2HCl=CuCl2+H2O
ó▄ēA+╦ß¹}+╦«
NaOH+HCl=NaCl+H2O
Ca(OH)2+H2SO4=CaSO4+2H2O
3HCl + Al(OH)3 = AlCl3 + 3H2O
ó▌*¹}+╦ßą┬¹}+ą┬╦ß
AgNO3+HCl=AgCl+HNO3
BaCl2+H2SO4=BaSO4+2HCl
Č■ĪóēA╝░ēAĄ─╗»īWąį┘|
ēAė╔ļxūėśŗ│╔Ż¼ēAį┌╦«╚▄ę║ųą─▄ĮŌļx│÷Įī┘ļxūė║═Üõč§Ė∙ļxūė(OH-)ĪŻ
│ŻęŖĄ─ēAėąÜõč§╗»Ōc(NaOH) ĪóÜõč§╗»Ō} Ca(OH)2Īó░▒╦«(NH3·H2O)Ą╚ĪŻ
1.Üõč§╗»ŌcĪóÜõč§╗»Ō}Ą─╬’└Ēąį┘|Īóė├═Š
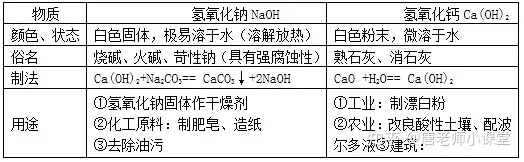
2.ēAĄ─╗»īWąį┘|
ūŽ╔½╩»╚’įćę║ė÷ēA╚▄ę║ūā╦{Ż¼¤o╔½Ęė╠¬įćę║ė÷ēA╚▄ę║ūā╝tĪŻ
ó┘╦ßąįč§╗»╬’+ēA¹}+╦«
2NaOH+CO2=Na2CO3+H2O
*2NaOH+SiO2=Na2SiO3+H2O
Ca(OH)2+CO2=CaCO3+H2O
ó┌╦ß+ēA¹}+╦«(ųą║═Ę┤æ¬)
ó█*¹}+ēAą┬¹}+ą┬ēA(Ę┤æ¬╬’Š∙┐╔╚▄)
2NaOH+CuSO4=Na2SO4+Cu(OH)2
╚²Īó¹}Ą─ąį┘|
1.│ŻęŖĄ─¹}
¹}ė╔ļxūėśŗ│╔Ż¼ĮM│╔└’║¼ėąĮī┘ļxūė(╗“NH4+)║═╦ßĖ∙ļxūėĄ─ę╗ŅÉ╗»║Ž╬’ĪŻ
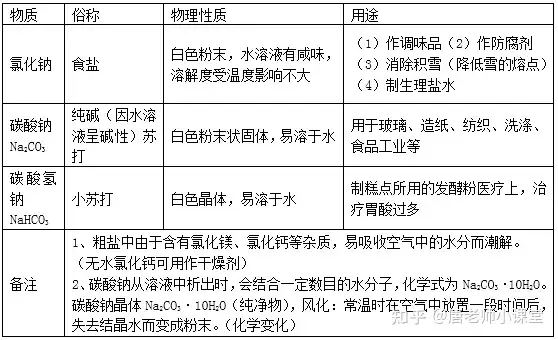
2.┤ų¹}╠ß╝ā
╚ź│²┤ų¹}ųą▓╗╚▄ąįļs┘|ĪŻ
3.¹}Ą─╗»īWąį┘|
ó┘¹}╚▄ę║+Įī┘ą┬¹}+ą┬Įī┘(░┤Įī┘╗ŅäėąįĒśą“)
CuSO4+Zn=ZnSO4+Cu
CaCO3+2HCl=CaCl2+H2O+CO2
Na2CO3+2HCl=2NaCl+H2O+CO2
NaHCO3+HCl=NaCl+H2O+CO2
¹}╚▄ę║+ēA╚▄ę║ą┬¹}+ą┬ēA(▒žėąę╗éĆ╩Ū│┴ĄĒ)
Ca(OH)2+Na2CO3==CaCO3+2NaOH(├„ąŪĘ┤æ¬)
3NaOH+FeCl3=3NaCl+Fe(OH)3
¹}╚▄ę║+¹}╚▄ę║ą┬¹}+ą┬¹}(▒žėąę╗éĆ╩Ū│┴ĄĒ)
CaCl2+Na2CO3=CaCO3+2NaCl
AgNO3+NaCl=AgCl+NaNO3
╦─Īó├„┤_Å═ĘųĮŌĘ┤æ¬░l╔·Ą─▒Š┘|
Å═ĘųĮŌĘ┤æ¬Ż║ė╔ā╔ĘN╗»║Ž╬’(═©│Ż×ķ╦ßēA¹})ŽÓ╗źĮ╗ōQ│╔ĘųŻ¼╔·│╔┴Ē═Ōā╔ĘN╗»║Ž╬’Ą─Ę┤æ¬ĪŻ
═©╩ĮŻ║AB+CD=AD+CB
░l╔·Ą─Śl╝■Ż║╔·│╔╬’ųą╚ń╣¹ėąĪó╗“ėąH2O(ĘĆČ©Īóļy╚▄ĪóļyļŖļx╬’┘|)
ūóęŌŻ║ēA┼cč§╗»╬’Ą─Ę┤æ¬▓╗ī┘ė┌Å═ĘųĮŌĘ┤æ¬
ī”ė┌Å═ĘųĮŌĘ┤æ¬Ą─╚²┤¾╠ž³cę▓╩Ū═¼īWéā▒žĒÜę¬ėøūĪĄ─Ż¼Ą┌ę╗Ę┤æ¬╬’Ż¼╔·│╔╬’Š∙ų╗ėąā╔ĘN╗»║Ž╬’ĪŻĄ┌Č■Ż¼░l╔·Ę┤æ¬Ą─ā╔ĘN╗»║Ž╬’ŽÓ╗źĮ╗ōQ│╔ĘųŻ¼╚²éĆį¬╦žĄ─╗»║Žārį┌Ę┤æ¬Ą─Ū░║¾Š∙▓╗░l╔·Ė─ūāŻ¼═¼īWéāį┌┼ąöÓ╩Ūʱ╩ŪÅ═ĘųĮŌĘ┤æ¬ĢrŻ¼ų╗ąĶę¬ę└ō■ęį╔ŽĄ─Śl╝┤┐╔▒µäeĪŻ
╬ÕĪó╩ņėø╦ßĪóēAĪó¹}Ą─╚▄ĮŌąį┐┌įE
ēA╚▄░▒ĪóŌcĪóŌøĪóõ^ĪóŌ}(░│─├╝┘▒╗╔w)
ŌøŌcõ@(õ@¹})Ž§(Ž§╦ß¹})╚½Č╝╚▄ĪŻ
┴“╦ß¹}▓╗╚▄õ^║═ŃU;┬╚╗»╬’▓╗╚▄Ńyüå╣»Ż¼╠╝╦ß¹}ų╗╚▄ŌøŌcõ@ĪŻ
┴∙ĪóÄūéĆ│ŻęŖļxūėĄ─Öz“×
1.Cl-ļxūėĄ─Öz“× (▀x)
╚Ī╔┘┴┐śėŲĘė┌įć╣▄ųąŻ¼Ą╬╝ėAgNO3╚▄ę║║═ŽĪHNO3ėą▓╗╚▄ė┌ŽĪŽ§╦ߥ─░ū╔½│┴ĄĒ╔·│╔Ż¼śėŲĘ║¼ėąCl-Ż¼ AgNO3+KCl=AgCl+KNO3
2.SO42-ļxūėĄ─Öz“× (▀x)
╚Ī╔┘┴┐śėŲĘė┌įć╣▄ųąŻ¼Ą╬╝ėBa(NO3)2╚▄ę║║═ŽĪHNO3ėą▓╗╚▄ė┌ŽĪŽ§╦ߥ─░ū╔½│┴ĄĒ╔·│╔Ż¼śėŲĘ║¼ėąSO42-Ż¼ Ba(NO3)2+H2SO4=BaSO4+2HNO3
3. CO32-ļxūėĄ─Öz“×
╚Ī╔┘┴┐śėŲĘė┌įć╣▄ųąŻ¼Ą╬╝ėŽĪHClŻ¼īó╔·│╔Ą─ÜŌ¾w═©╚ļ│╬ŪÕ╩»╗ę╦«ėą¤o╔½ÜŌ¾w╔·│╔Ż¼įōÜŌ¾w╩╣│╬ŪÕ╩»╗ę╦«ūā£åØ߯¼śėŲĘ║¼ėąCO32-Ż¼
K2CO3+2HCl=2KCl+CO2+H2O
CO2+Ca(OH)2=CaCO3+H2O
4.Öz“×NH4+(▀x)
╚Ī╔┘┴┐┤²Öz╬’ė┌ØŹā¶Ą─įć╣▄ųąŻ¼Ą╬╚ļ▀m┴┐NaOH╚▄ę║▓ó╝ė¤ßŻ¼ėą╩╣رĄ─╝t╔½╩»╚’įć╝łūā│╔╦{╔½Ą─ÜŌ¾w«a╔·ĪŻ
5ĪóĶbäeŽĪ¹}╦ß║═ŽĪ┴“╦ß
Ęųäe╚Ī╔┘┴┐┤²Özę║¾wė┌ā╔ų¦ØŹā¶Ą─įć╣▄ųąŻ¼Ė„Ą╬╚ļÄūĄ╬BaCl2╚▄ę║Ż¼ėą░ū╔½│┴ĄĒ«a╔·Ą─įŁ╚▄ę║╩ŪŽĪ┴“╦߯¼¤o¼FŽ¾«a╔·Ą─įŁ╚▄ę║╩ŪŽĪ¹}╦ßĪŻ
Ų▀Īó│ŻęŖ╦ūĘQĪó│╔Ęų║═╗»īW╩Į
╔·╩»╗ę——CaO ╩ņ╩»╗ę——Ca(OH)2
╩»╗ę╩»Īó┤¾└Ē╩»——CaCO3╩│¹}——NaCl
╗ēAĪó¤²ēAĪó┐┴ąįŌc——NaOH ╝āēAĪó╠K┤“——Na2CO3 ąĪ╠K┤“——NaHCO3
ĶFõPĪó│ÓĶFĄV——Fe2O3 ┤┼ĶFĄV——Fe3O4 Įäé╩»Īó╩»─½——C Ė╔▒∙——CO2 ▒∙——H2O ╠ņ╚╗ÜŌ(╝ū═ķ)——CH4
ŠŲŠ½(ęę┤╝)——C2H5OH ┤ū╦ß(ęę╦ß)——CH3COOH
░╦Īó│ŻęŖ╬’┘|Ą─Ņü╔½
╝t╔½Ą─╣╠¾w——CuĪóFe2O3ĪóP(╝t┴ū)
║┌╔½Ą─╣╠¾w——CĪóCuOĪóFe3O4ĪóFeOĪóMnO2
░ū╔½Ą─╣╠¾w——KClO3ĪóP2O5ĪóP(░ū┴ū)ĪóCuSO4(¤o╦«┴“╦ßŃ~)ĪóKClĪóNaClĄ╚
░ĄūŽ╔½Ą─╣╠¾w——KMnO4
ĄŁ³S╔½Ą─╣╠¾w——S
╦{╔½Š¦¾w——CuSO4•5H2O
╦{╔½│┴ĄĒ——Cu(OH)2
╝t║ų╔½│┴ĄĒ——Fe(OH)3
░ū╔½│┴ĄĒ(▓╗╚▄ė┌╦ß)——BaSO4ĪóAgCl
░ū╔½│┴ĄĒ(╠╝╦ß¹})——CaCO3ĪóBaCO3
░ū╔½│┴ĄĒ(ēA)——Mg(OH)2ĪóAl(OH)3
╦{╔½╚▄ę║——CuSO4ĪóCu(NO3)2Ą╚║¼Cu2+╚▄ę║
£\ŠG╔½╚▄ę║——FeSO4ĪóFeCl2Ą╚║¼Fe2+╚▄ę║
ūž³S╔½╚▄ę║——FeCl3ĪóFe2(SO4)3Ą╚║¼Fe3+╚▄ę║
ī”ė┌│§ųąļAČ╬╦ßēA¹}Ą─īW┴ĢŻ¼Ųõ░³║¼Ą─ā╚╚▌┴┐▀Ć╩Ū▒╚▌^ČÓĄ─Ż¼─Ū├┤į┌īW┴Ģ«öųąŽļę¬┐ņ╦┘Ą─šŲ╬š▀@▓┐ĘųĄ─ā╚╚▌Ż¼─Ū├┤ī”Ųõ╚½├µĄ─┴╦ĮŌ═ŌŻ¼▀Ćę¬ßśī”├┐ę╗▓┐ĘųĄ─ā╚╚▌▀Mąą╝Üų┬Ą─Ęų╬÷Ż¼╠žäeŲõųą╔µ╝░ĄĮĄ─ę╗ą®║åå╬Ą─īŹ“×─▄ę▓─▄ē“Ä═ų·┤¾╝ę┐ņ╦┘Ą─šŲ╬š╦ßēA¹}Ė„▓┐ĘųĄ─ąį┘|ĪŻŲõųąųžę¬Ą─ę╗ą®╗»īWĘĮ│╠╩ĮĪŻėøæøĄ─┐┌įEČ╝╩Ū┤¾╝ęį┌īW┴Ģ╗“Å═┴Ģ«öųą▒╚▌^ųžę¬Ą─īW┴Ģā╚╚▌ĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖCĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠWŻ¼2025ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³cō¶▓ķ┐┤